Хімічні властивості та застосування неметалів
- 15-11-2023, 05:52
- 377
11 клас , Хімія 11 клас Попель, Крикля (рівень стандарту)
§ 17. Хімічні властивості та застосування неметалів
Матеріал параграфа допоможе вам:
- дізнатися про характерну роль неметалів в окисно-відновних реакціях;
- визначати окисник і відновник у реакціях за участю неметалів;
- отримати інформацію про сфери застосування неметалів.
Хімічні властивості. Неметали мають багато спільних хімічних властивостей. Вони взаємодіють з металами, між собою, зі складними речовинами різних класів. Ці реакції належать до окисно-відновних реакцій.
Неметали як окисники. Оскільки атоми неметалічних елементів здатні приєднувати електрони, то для неметалів характерна роль окисника. Найактивнішими окисниками є прості речовини найбільш електронегативних елементів — фтор, озон, кисень, хлор.
Цікаво знати
За добування й дослідження «найагресивнішого» неметалу фтору французький учений А. Муассан у 1906 р. отримав Нобелівську премію з хімії.
Неметали є окисниками в усіх реакціях з металами. Більшість таких реакцій відбувається з високою швидкістю, виділенням значної кількості теплоти, а іноді з’являється полум’я (мал. 36).

Мал. 36. Горіння натрію у хлорі
• Складіть рівняння реакцій літію із сіркою, алюмінію з киснем.
Роль окисника виконують неметали і в реакціях з воднем — простою речовиною Гідрогену, який має досить низьку електронегативність. Атоми Гідрогену в цих хімічних перетвореннях втрачають електрони й виступають відновником.
Цікаво знати
Бор і силіцій не взаємодіють із воднем. Проте сполуки відповідних елементів із Гідрогеном відомі.
Чим більша електронегативність неметалічного елемента, тим активніше його проста речовина реагує з воднем. Яскравий приклад цієї закономірності — взаємодія галогенів із воднем. Загальне рівняння такої реакції:
Е2 + Н2 = 2HE.
Фтор реагує з воднем із вибухом, хлор — з аналогічним ефектом, але при освітленні (у темряві хлор і водень не взаємодіють). Реакції брому і йоду з воднем відбуваються лише при нагріванні й не призводять до повного витрачання речовин.
Неметали як відновники. Виявлення відновних властивостей слід очікувати передусім від неметалів, які походять від найменш електронегативних неметалічних елементів, — водню Н2 і вуглецю С. Ці речовини є відновниками у реакціях з галогенами, киснем, сіркою, азотом. Водень, вуглець, чимало інших неметалів горять у кисні або на повітрі. Продукти таких реакцій — оксиди. Якщо неметалічний елемент має змінну валентність, то за нестачі кисню часто утворюється оксид із нижчим ступенем окиснення елемента, а за надлишку кисню — вищий оксид:
2С + О2 (нест.) = 2СО; С + О2 (надл.) = СО2.
Цікаво знати
Водень і вуглець не реагують з оксидами лужних елементів, Барію, Алюмінію.
Водень і вуглець як відновники взаємодіють з оксидами металічних елементів. Відповідні реакції використовують у металургії. На них, зокрема, ґрунтується виробництво заліза. Наводимо схеми деяких реакцій, які здійснюють на металургійних заводах:
![]()
• Перетворіть схеми реакцій на хімічні рівняння.
Застосування. Більшість неметалів є важливими для практики. Про галузі використання кисню ви довідались у 7 класі. Озон і хлор з огляду на їхні бактерицидні властивості застосовують для знезараження води. Хлор є вихідною речовиною у виробництві хлорного вапна, органічних розчинників, засобів захисту рослин від хвороб і шкідників.
Графіт завдяки шаруватій будові слугує змащувальним матеріалом, а його електропровідність дає змогу виготовляти електричні контакти й електроди. Стержні з графіту застосовують у ядерних реакторах. Алмазний порошок використовують у шліфувальних і різальних інструментах (мал. 37). Обробляючи прозорі алмази, виготовляють діаманти.

Мал. 37. Різальна машина
Водень є сировиною для хімічної й нафтопереробної промисловості. Силіцій як напівпровідник використовують в електронній техніці, сонячних батареях (мал. 38). Хімічно пасивним газом азотом наповнюють колби електричних ламп. З азоту і водню добувають амоніак, а з нього — нітратну кислоту, азотні добрива. Азот, аргон і гелій використовують у техніці й наукових дослідженнях як інертне газове середовище для запобігання окисненню речовин киснем повітря.

Мал. 38. Сонячні батареї на даху будинку
Природна сірка слугує вихідною речовиною у виробництві сульфатної кислоти. Її додають у каучук для перетворення його на гуму. Фосфор використовують при виготовленні сірників.
• Розчин якого неметалу є дезінфекційним засобом? Яка назва цього засобу і який розчинник міститься в ньому?
ВИСНОВКИ
Неметали в хімічних реакціях є переважно окисниками. Вони взаємодіють із металами, між собою. Водень і вуглець як відновники реагують з оксидами металічних елементів; за допомогою цих реакцій добувають метали.
Більшість неметалів використовують у техніці, хімічній промисловості.
- 120. Який неметал у хімічних реакціях є лише окисником? Чи існують неметали, яким притаманні тільки відновні властивості? Відповіді обґрунтуйте.
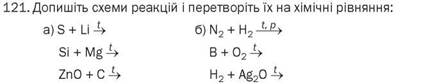
- 122. Сірка вступає в реакції з воднем і киснем. Напишіть відповідні хімічні рівняння, складіть схеми окиснення й відновлення. Яку роль виконує Сульфур у кожній реакції?
- 123. Складіть рівняння реакції фтору з водою, врахувавши, що одним із продуктів є проста речовина, поширена в атмосфері.
- 124. Вуглець за високої температури реагує з водяною парою. Які речовини мають бути продуктами цієї реакції — CO і Н2 чи СН4 і О2? Відповідь обґрунтуйте, наведіть відповідне хімічне рівняння.
- 125. Складіть рівняння реакцій хлору з калієм, цинком, алюмінієм, силіцієм, фосфором. Зважте на те, що Силіцій і Фосфор у продуктах відповідних реакцій мають найвищі ступені окиснення.
- 126. Запишіть замість крапок відповідні цифри і слова:
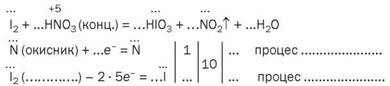
- 127. Перетворіть схеми реакцій на хімічні рівняння, скориставшись методом електронного балансу:
а) Si + NaOH + Н2О → Na2SiO3 + Н2↑;
б) S + H2SO4 (конц.) → SO2↑ + Н2О.
- 128. Між двома найактивнішими галогенами можуть відбуватися реакції з утворенням сполук АБ, АБ3 і АБ5. Розшифруйте формули сполук, записавши в них символи елементів. Візьміть до уваги, що кожна літера відповідає певному галогену. Поясніть свій вибір.
Коментарі (0)