Завдання різного рівня складності. Періодичний закон і періодична система хімічних елементів
- 15-11-2023, 21:59
- 252
11 клас , Хімія 11 клас Ярошенко (рівень стандарту)
§ 4. Завдання різного рівня складності
1. Укажіть протонне число s-елемента.
А 6
Б 11
В 13
Г 16
2. Укажіть протонне число р-елемента.
А 20
Б 26
В 19
Г 17
3. Укажіть протонне число d-елемента.
А 10
Б 15
В 20
Г 26
4. Укажіть символ хімічного елемента, електронна конфігурація зовнішнього енергетичного рівня якого 2s22p5.
А Cr
Б N
В P
Г F
5. Укажіть назву хімічного елемента за його електронною формулою 1s22s22p63s23p5.
А Нітроген
Б Оксиген
В Сульфур
Г Хлор
Збуджений чи основний стан атома передає ця електронна формула?
6. Укажіть електронну формулу атома, що перебуває у збудженому стані.
А 1s22s22p63s1
Б 1s22s22p63s23p33d1
В 1s22s2
Г 1s22s22p63s23p6
7. Визначте характерну ознаку елемента, розташованого у 3 періоді й V групі періодичної системи.
А у збудженому стані має електронну конфігурацію 1s22s22p63s23p5
Б належить до d-елементів
В максимальний ступінь окиснення +5
Г заряд ядра атома +12
8. Укажіть назву хімічного елемента, у атома якого в основному стані найбільше неспарених електронів.
А Неон
Б Натрій
В Карбон
Г Нітроген
9. Укажіть електронну конфігурацію атома Карбону у збудженому стані.
А 1s22s22p2
Б 1s22s22p63s23p1
В 1s22s12p3
Г 1s22s22p5
10. Укажіть назву хімічного елемента, у атомі якого всі електрони в основному стані спарені.
А Неон
Б Хлор
В Карбон
Г Сульфур
11. Схожі властивості з Натрієм має хімічний елемент з електронною формулою атома...
А 1s22s22p2
Б 1s22s1
В 1s22s22p3
Г 1s22s22p6
12. Проаналізуйте твердження 1 і 2 й виберіть правильний варіант відповіді.
1. Кількість електронів на зовнішньому енергетичному рівні атомів елементів головних підгруп збігається з номером групи.
2. Кількість електронів в електронній оболонці атома збігається з атомним номером елемента.
А правильне лише твердження 1
Б правильне лише твердження 2
В правильні обидва твердження
Г неправильні обидва твердження
13. Проаналізуйте твердження 1 і 2 й виберіть правильний варіант відповіді.
1. У переліку Карбон, Бром, Оксиген, Магній, Флуор, Літій, Хлор переважають елементи з однаковою електронною формулою зовнішнього енергетичного рівня атома в основному стані.
2. Електронні оболонки атомів Натрію, Фосфору, Сульфуру, Аргону мають однакову кількість енергетичних рівнів.
А правильне лише твердження 1
Б правильне лише твердження 2
В правильні обидва твердження
Г неправильні обидва твердження
14. Проаналізуйте твердження 1 і 2 й виберіть правильний варіант відповіді.
1. В електронних конфігураціях атомів Калію і Феруму різна кількість енергетичних рівнів.
2. Атоми Калію і Феруму мають однакову кількість електронів на зовнішньому енергетичному рівні.
А правильне лише твердження 1
Б правильне лише твердження 2
В правильні обидва твердження
Г неправильні обидва твердження
15. Проаналізуйте твердження 1 і 2 й виберіть правильний варіант відповіді.
1. Валентними електронами в атомі Феруму є d- і р-електрони.
2. Для Карбону і Силіцію можливими є ступені окиснення +2 і +4.
А правильне лише твердження 1
Б правильне лише твердження 2
В правильні обидва твердження
Г неправильні обидва твердження
16. Розташуйте назви хімічних елементів за збільшенням кількості неспарених електронів у їхніх атомах в основному стані.
А Бор
Б Фосфор
В Ферум
Г Оксиген
17. Розташуйте елементи за збільшенням кількості s-електронів в їхніх атомах.
А Натрій
Б Нітроген
В Кальцій
Г Сульфур
18. Укажіть спільні характеристики атомів Оксигену й Сульфуру.
А однакова кількість енергетичних рівнів
Б однакова кількість електронів на зовнішньому енергетичному рівні
В однаковий вищий ступінь окиснення
Г належать до р-елементів
19. Розташуйте формули бінарних сполук Хлору за збільшенням його ступеня окиснення.
А Cl2O
Б Cl2O7
В Cl2O5
Г HCl
Чим ви можете пояснити таку різноманітність ступенів окиснення Хлору?
20. Установіть відповідність між загальною електронною формулою зовнішнього енергетичного рівня атомів хімічних елементів однієї головної підгрупи і номером групи.
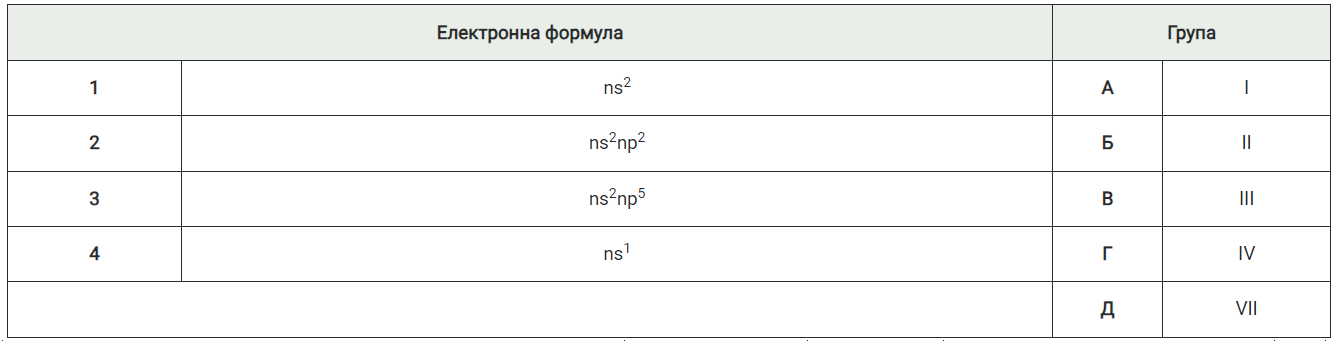
21. Складіть формулу оксигеновмісної кислоти, у якій Сульфур має максимальний ступінь окиснення.
22. Про який валентний стан Фосфору свідчать формули двох його кислот: НРО3 та Н3РО4?
23. Класифікуйте елементи на групи s-, р-, d-елементів: Магній, Алюміній, Ферум, Нітроген, Гідроген, Флуор.
Коментарі (0)