Фізичні властивості неметалів. Алотропія
- 14-11-2023, 15:09
- 249
11 клас , Хімія 11 клас Лашевська (рівень стандарту)
§ 16. Фізичні властивості неметалів. Алотропія
Після опрацювання параграфа ви зможете:
- характеризувати фізичні властивості неметалів та встановлювати залежність їхніх властивостей від будови;
- пояснювати суть явища алотропії; відмінності властивостей алотропних модифікацій Оксигену їхнім кількісним складом та будовою;
- наводити приклади алотропних модифікацій Оксигену;
- обґрунтовувати значення алотропних перетворень;
- висловлювати судження щодо біологічної ролі озону та його застосування.
Фізичні властивості неметалів розмаїті та зумовлені особливостями їхнього складу та будови. Знати ці властивості необхідно як для ефективного використання традиційних матеріалів і технологій, так і для створення новітніх.
Неметали молекулярної будови мають невисокі температури плавлення, оскільки сили притягання між їхніми молекулами досить слабкі. Наприклад, кисень, фтор, хлор скраплюються та тверднуть за від’ємних температур. Бром - летка рідина, а внаслідок нагрівання кристалів йоду відбувається їхня сублімація (див. § 8, рис. 8.6).
Інертні елементи за звичайних умов існують у вигляді атомів, оскільки мають завершений зовнішній енергетичний рівень. У решти простих речовин-неметалів атоми сполучені між собою ковалентними неполярними зв’язками. Деякі неметалічні елементи утворюють двохатомні молекули (наведіть кілька прикладів).
У молекулах водню та галогенів зв’язки між атомами ординарні, у молекулі кисню зв’язок між атомами Оксигену подвійний, у молекулі азоту атоми Нітрогену сполучені потрійним зв’язком (рис. 16.1).
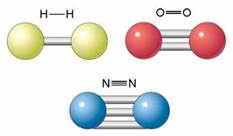
Рис. 16.1. Будова молекул деяких неметалів. Ідентифікуйте їх
Розгляньмо докладніше фізичні властивості азоту - головного складника повітря.
• З огляду на те, що ви знаєте про азот з повсякденного життя, заповніть прогалини в тексті, наведеному далі.
Молекула азоту неполярна, тож цей газ ... розчиняється у воді. Сили взаємодії між молекулами азоту дуже ..., тому за звичайних умов ця речовина перебуває в ... стані. Він прозорий, ..., не має смаку та ... . За температури -195,8 °С азот перетворюється на безбарвну, рухливу, як вода, ... . Унаслідок кристалізації азоту за температури -209,86 °С утворюється біла снігоподібна маса або великі білосніжні кристали. Рідкий азот застосовують як охолоджувач та в кріотерапії (рис. 16.2).

Рис. 16.2. Рідкий азот застосовують у лабораторіях, на виробництві, у медицині як ефективний охолоджувач. 1. Зберігання біологічного матеріалу в посудинах з рідким азотом. 2. Кріохірургія - ефективний метод видалення новоутворень на шкірі
Неметали, які мають атомні кристалічні ґратки, вирізняються твердістю та тугоплавкістю (поясніть чому). Наприклад, температура плавлення силіцію становить 1410 °С, кристали бору плавляться за 2075 °С, а температура кипіння цієї речовини - понад 3500 °С.
Неметали непластичні, поміж них переважають діелектрики, хоча зрідка трапляються й напівпровідники та провідники електричного струму. Дізнатися більше про фізичні властивості неметалів можна з таблиці 1 Додатка.
Скільки загалом неметалів? Очевидно, що їхня кількість більша за кількість неметалічних елементів. Адже в природі є прості речовини, які істотно відрізняються одна від одної за своїми властивостями, хоча й утворені атомами одного неметалічного елемента. З курсу хімії основної школи ви знаєте, що Оксиген утворює прості речовини кисень та озон. Такі речовини називають алотропними модифікаціями (видозмінами), а явище їхнього існування - алотропією.
Цікаво і пізнавально
Термін «алотропія» 1841 року запровадив Й. Я. Берцеліус, слово «алотропія» походить від давньогрецьких слів άλλος - інший і τροπος - поворот, властивість.
Чому речовини-алотропи мають різні властивості, хоча утворені атомами того самого елемента? Пригадаймо: причини відмінностей у властивостях, які ми спостерігаємо на рівні макросвіту, потрібно шукати на рівні мікросвіту. Алотропні модифікації можуть відрізнятися одна від одної кількісним складом. Наприклад, молекули кисню О2 та озону О3 складаються з різної кількості атомів Оксигену. Наслідком цього є те, що кисень не має запаху, а озон дістав свою назву саме через характерний запах. Дізнатися більше про подібність і відмінність алотропних модифікацій Оксигену ви зможете з таблиці 2 Додатка.
Чи здатні алотропні модифікації взаємоперетворюватися? З кисню в тихому (без світіння та іскр) електричному розряді утворюється озон:
О2 ⇄ О3; ΔΗ > 0.
• Перетворіть схему реакції алотропного перетворення кисню на хімічне рівняння, проаналізуйте його. Класифікуйте її за тепловим ефектом та ознакою оборотності. Як уплине на хімічну рівновагу цієї реакції підвищення температури та тиску? Чому?
Цікаво і пізнавально
Уперше озон виявив у 1785 році голландський фізик М. ван Марум за характерним запахом і окиснювальними властивостями. Термін «озон» (від грец. Όζω - пахну) запропонував німецький хімік Х. Ф. Шенбейн у 1840 році.
У природі вміст озону в повітрі зростає під час грози, унаслідок цього ми відчуваємо характерний свіжий запах. Найбільше озону утворюється в стратосфері, на висоті 12-50 км, під упливом ультрафіолетового випромінювання Сонця. Загальний уміст озону в атмосфері відповідає шару цього газу завтовшки 3 мм (за стандартного тиску).
Корисний чи шкідливий озон? Озоновий шар захищає організми від шкідливого ультрафіолетового випромінювання (рис. 16.3). Тому стратегії збалансованого розвитку людства передбачають захист озонового шару від руйнування. Про важливість цього завдання свідчить те, що 1994 року Генеральна Асамблея ООН проголосила 16 вересня Міжнародним днем охорони озонового шару. Тож під час купівлі аерозольних балончиків, кондиціонера чи холодильника звертайте увагу на марковання товарів. Вибравши товари та технології, використання яких не завдає шкоди озоновому шару, ви не лише дбатимете про власне здоров’я та здоров’я нащадків, а й про збереження життя на Землі.

Рис. 16.3. Озоновий шар захищає організми від шкідливого ультрафіолетового випромінювання
Знезаражування питної води озоном має низку переваг порівняно з хлоруванням. У медицині озон використовують для дезінфікування та стерилізування. Озонотерапія - новий високоефективний метод лікування, який застосовують у найрізноманітніших галузях медицини. Тому важливо знати властивості цієї алотропної модифікації Оксигену, щоб безпечно використовувати її на благо людини. Адже озон - дуже агресивна й отруйна речовина. Підвищення вмісту в повітрі озону техногенного походження небезпечне для організмів. Унаслідок дії озону пришвидшується старіння конструкційних матеріалів, руйнуються художні фарби - їхні кольори тьмяніють. Тому підвищений уміст цього газу в повітрі небезпечний не лише для організмів, а й для витворів мистецтва.
Докладніше про алотропію деяких інших неметалічних елементів ітиметься в наступному параграфі.
https://www.youtube.com/watch?v=Gz3lrLoW0og
https://www.youtube.com/watch?v=mVhObSZUQM0
https://www.youtube.com/watch?v=dB6Dxsxb8Og
ПРО ГОЛОВНЕ
• Неметали молекулярної будови мають невисокі температури плавлення.
• Неметали з атомними кристалічними ґратками вирізняються твердістю та тугоплавкістю.
• Неметали непластичні, поміж них переважають діелектрики, хоча зрідка трапляються й напівпровідники та провідники електричного струму.
• Алотропія - явище існування одного хімічного елемента у вигляді кількох простих речовин з різними властивостями - алотропних модифікацій.
• Алотропні модифікації здатні взаємоперетворюватися.
• Озон О3 і кисень О2 - алотропні модифікації Оксигену.
• Озоновий шар захищає організми від шкідливого ультрафіолетового випромінювання.
Перевірте себе
- 1. Перетворіть розповідні речення рубрики ПРО ГОЛОВНЕ на питальні. Чи можете ви відповісти на ці запитання без допомоги підручника?
Застосуйте свої знання й уміння
- 2. Розчинність озону у воді за 0 °С - 0,394 кг/м3 (0,494 л/кг), що вдесятеро вища за розчинність кисню. Порівняйте будову молекул кисню (рис. 16.2) та озону й поясніть цей факт.
- 3. Електрофільтр - це пристрій, у якому очищення газів від аерозольних, твердих або рідких частинок відбувається під дією електричних сил. У результаті дії електричного поля частинки, які набувають заряду в полі коронного розряду, осідають на електродах. Поясніть, чому: а) не рекомендовано використовувати електрофільтри для очищення повітря в музеях; б) тиглі, у яких плавлять золото, виготовляють з графіту.
![]()
Творча майстерня
- 5. Розробіть для молодшого учнівства сценарій театралізованої вистави «Озон: користь і шкода» та втільте його в життя.
Коментарі (0)