Оксиди неметалічних елементів, їхній уміст в атмосфері. Кислотні дощі
- 14-11-2023, 22:45
- 370
11 клас , Хімія 11 клас Лашевська (рівень стандарту)
§ 21. Оксиди неметалічних елементів, їхній уміст в атмосфері. Кислотні дощі
Після опрацювання цього параграфа ви зможете:
- називати кислотні оксиди за систематичною номенклатурою;
- складати рівняння реакцій, які характеризують хімічні властивості та добування кислотних оксидів;
- пояснювати антропогенні й природні причини появи в атмосфері оксидів неметалічних елементів;
- висловлювати судження щодо екологічних наслідків викидів в атмосферу оксидів Карбону, Нітрогену, Сульфуру; кислотних дощів.
Оксиди неметалічних елементів досить добре відомі вам з повсякденного життя. Гідроген оксид - головний складник нашого організму. Карбон(ІV) оксид - продукт газообміну в легенях людини й сировина для фотосинтезу глюкози й крохмалю рослинами. Карбон(ІІ) оксид - надзвичайно небезпечна сполука, унаслідок отруєння якою під час пожеж гинуть люди. Різкий характерний запах сульфур(ІV) оксиду відчували ті, хто запалював сірника. І чи не кожний чи кожна з вас загоряли на пляжах, устелених безліччю дрібних кристаликів силіцій(ІV) оксиду.
• Запишіть хімічні формули оксидів, назви яких наведено в попередньому абзаці. Зазначте ступені окиснення хімічних елементів у них.
Здебільшого неметалічні елементи утворюють по декілька оксидів (наведіть кілька прикладів). Продуктами реакцій багатьох оксидів неметалічних елементів з водою є кислоти (доповніть наведені далі схеми хімічних реакцій):
SO2 + Н2О ⇄ ...;
Ν2Ο5 + Н2О → ... .
Ви, напевно, звернули увагу, що елемент Е кислотного оксиду ЕхОу під час утворення кислоти переходить до складу аніона. Те саме відбувається й під час утворення солей у реакціях з лугами, основними оксидами та деякими солями. Так, під дією карбон(ІV) оксиду вапняна вода - прозорий насичений розчин кальцій гідроксиду - стає каламутною внаслідок утворення кальцій карбонату:
СО2 + Са(ОН)2 = ...↓ + Н2О (рис. 21.1.1).
Сплавлянням кварцового піску з лугом можна добути натрій силікат - так зване розчинне скло (рис. 21.1.2):
![]()

Рис. 21.1. 1. Пропускання карбон(ІV) оксиду крізь вапняну воду. 2. Розчинне скло - водний розчин продукту сплавляння силіцій(ІV) оксиду з натрій гідроксидом
• Класифікуйте ці реакції за кількістю реагентів і продуктів, перетворіть схему реакції силіцій(ІV) оксиду з натрій гідроксидом на хімічне рівняння. Наведіть ще кілька прикладів на підтвердження зазначеного вище.
Кислотні оксиди реагують з основними оксидами, а нелеткі кислотні оксиди під час сплавляння витісняють із солей леткі оксиди (перетворіть наведені далі схеми реакцій на хімічні рівняння):
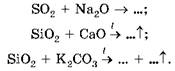
Способи добування кислотних оксидів вам також відомі, ви самостійно зможете їх схарактеризувати (зробіть це), проаналізувавши наведені далі схеми хімічних реакцій, перетворивши їх на хімічні рівняння та класифікувавши за кількістю реагентів і продуктів та з погляду окиснення-відновлення1:
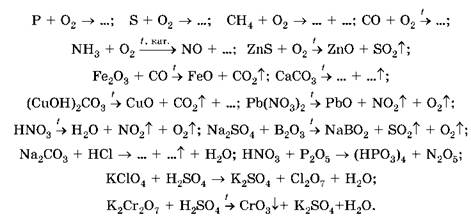
1 Які саме схеми реакцій опрацювати, вам порадить учитель або вчителька хімії.
• Які з наведених схем реакцій описують загальні методи добування кислотних оксидів, а які - особливі? Які з них, на вашу думку, наведено лише для ознайомлення та застосування вже сформованих умінь?
Кислотні опади - одна з нагальних екологічних проблем сьогодення - утворюються внаслідок гідратації кислотних оксидів, які містяться в повітрі. Наприклад, карбон(ІV) оксид - один з його складників - розчиняється у воді та взаємодіє з нею під час формування й випадіння дощових крапель:
СO2 + Н2O ⇄ ... .
Продукт цієї реакції - слабка карбонатна кислота - зумовлює слабкокислу реакцію дощової води. Показник pH чистого дощу, який проходить крізь незабруднене повітря, у момент удару об землю становить 5,6 (порівняйте зі значенням показника pH дистильованої води).
Унаслідок вулканічної діяльності в повітря надходить сульфур(ІV) оксид. Під упливом електричних розрядів блискавки з азоту та кисню повітря утворюється нітроген(ІІ) оксид, який окиснюється до нітроген(ІV) оксиду (складіть рівняння цих реакцій).
Цікаво і пізнавально
Усі разом вулкани щороку викидають в атмосферу Землі від 20 до 35 млн тонн сульфур(ІV) оксиду. Це вдвічі менше від того обсягу, який потрапляє туди внаслідок людської діяльності.
Розкладання органічних решток унаслідок життєдіяльності мікроорганізмів також є джерелом надходження в атмосферу кислотних оксидів Карбону, Сульфуру, Нітрогену. Продукти їхньої гідратації підкислюють опади - дощі, сніги, тумани тощо.
Цікаво і пізнавально
На кисле середовище дощової води ще 1684 року звернув увагу англійський хімік і фізик Роберт Бойль. Термін «кислотний дощ» виник два століття потому, коли британські науковці зауважили, що забруднення повітря в промислово розвинутій центральній частині країни є причиною істотного підвищення кислотності опадів.
Небезпеку збільшення викидів кислотних оксидів техногенного походження (рис. 21.2) людство збагнуло лише в другій половині минулого століття.
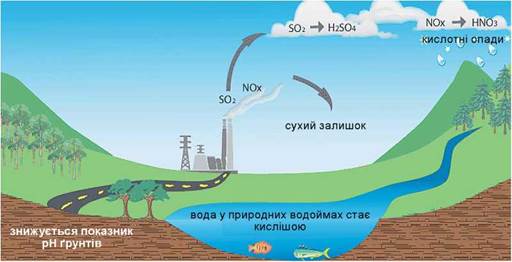
Рис. 21.2. Спалювання вугілля, нафти та нафтопродуктів на теплових електростанціях, у двигунах внутрішнього згоряння - джерела техногенного забруднення повітря кислотними оксидами
Цікаво і пізнавально
За даними Guardian, один великий круїзний лайнер викидає в атмосферу вуглекислого газу стільки само, як 83 тисячі автомобілів, оксидів Нітрогену - як 421 тисяча автомобілів, твердих дрібних частинок - як мільйон автомобілів і діоксиду Сульфуру - як 376 мільйонів автомобілів з двигуном внутрішнього згоряння.
Змоделюймо утворення кислотного дощу й дослідімо його вплив на об’єкти живої та неживої природи. Дослід виконуватимемо у витяжній шафі (поміркуйте чому). Зріжемо зі свіжого яблука смужку шкірки й покладемо її до порожньої термостійкої колби. Заповнимо ложечку для спалювання речовин на половину її об’єму сіркою. Запалимо сірку, зануримо ложечку в колбу й закриємо, наскільки це можливо, скляною пластинкою отвір посудини. Коли дим заповнить колбу, виймемо ложечку, повністю закриємо отвір колби скляною пластинкою й так само заповнимо сульфур(ІV) оксидом іншу, порожню колбу. Потім загасимо полум’я сірки в склянці з водою.
Через певний час ми побачимо, що шкірка яблука втратила пружність, стала зморшкуватою. Змінився також її колір - він утратив інтенсивність, наче «вицвів». Очевидно, сульфур(ІV) оксид «відняв» у яблучної шкірки воду й прореагував з рослинними барвниками, які містилися в її клітинах.
• Зробіть висновок щодо впливу кислотних оксидів і продуктів їхньої гідратації на рослини.
Цікаво і пізнавально
Рослини виявляють різну чутливість до сірчистого газу - сульфур(ІV) оксиду. Найчутливішими серед них є ялина та сосна, найменш чутливими - береза та дуб. З-поміж квітів найчутливіша до дії цього кислотного оксиду - троянда.
Добавимо в другу колбу дистильованої води об’ємом 10 мл, закоркуємо її та кілька разів струсимо. Помістимо краплю води зі змішаною бактеріальною культурою на предметне скло під мікроскоп. Піпеткою точнісінько в краплю з бактеріальною культурою добавимо три краплі рідини з колби. Під її впливом бактерії гинуть (поміркуйте, які ознаки мають свідчити про це).
• Зробіть висновок щодо впливу кислотних дощів на ґрунтові бактерії.
За зміною забарвлення універсального індикаторного папірця (якого кольору він набуває?) можна зробити висновок про те, що у водному розчині продукту гідратації сульфур(ІV) оксиду є катіони Гідрогену. Наслідком дії цього розчину на шматочок магнієвої стрічки є «розчинення» магнію та виділення бульбашок водню:
2Н+ + Mg0 = Mg2+ + H2↑.
• Складіть два молекулярні рівняння, що відповідають цьому скороченому йонному.
Аналогічні зміни відбуваються з кусочками мармуру, адже продуктами реакції є розчинна у воді сіль і газуватий карбон(ІV) оксид:
2Н+ + СаСО3 = Са2+ + CO2↑ + Н2О.

Рис. 21.3. Руйнівна дія кислотних опадів на об’єкти живої та неживої природи. 1. Мертвий ліс у Норвегії. 2. Мармуровий мавзолей-мечеть Тадж-Махал в Індії через кислотні дощі втрачає білосніжність
• 1. Складіть два молекулярні рівняння, що відповідають цьому скороченому йонному. 2. Роздивіться рисунок 21.3 і зробіть висновок щодо впливу кислотних дощів на рослини та історичні будівлі з мармуру та вапняку.
Звісно, тими ситуаціями, які ми змоделювали в лабораторних умовах, негативний уплив кислотних дощів не вичерпано. Унаслідок цього техногенного лиха підвищується кислотність ґрунтів - вони втрачають родючість, зменшується біологічне різноманіття видів організмів. Наприклад, неприродне підвищення вмісту катіонів Гідрогену у водоймах негативно впливає на здатність риб розмножуватися, призводить до їхньої масової загибелі.
Від кислотних опадів потерпають люди - кислотні оксиди Сульфуру й Нітрогену не лише подразнюють дихальні шляхи, слизові оболонки, руйнують зубну емаль, а й спричиняють хронічне отруєння організму та, як наслідок, зниження імунітету.
Кислотні опади вимивають з гірських порід, ґрунтів, донних покладів катіони Алюмінію, важких металічних елементів, зокрема Меркурію. Унаслідок цього вони стають складниками ланцюгів живлення, що призводить до хронічного, а трапляється, і гострого отруєння організмів.
Як запобігти утворенню кислотних опадів і компенсувати наслідки їхньої руйнівної дії? Частково зарадити лиху можна очищенням палива від домішок сульфуровмісних сполук, а продуктів спалювання - від кислотних оксидів. Якщо спалювання здійснювати за нижчих температур, зменшується утворення оксидів Нітрогену. Для очищення від них ефективним є каталітичне відновлення за участю амоніаку1 (використавши метод електронного балансу, перетворіть наведені далі схеми реакцій на хімічні рівняння):
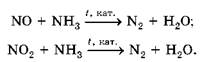
1 Інформацію наведено для ознайомлення та опрацювання, а не для запам’ятовування.
• 1. Проаналізуйте склад продуктів двох реакцій, рівняння яких наведено вище, і поясніть, чому цей спосіб видалення домішок оксидів Нітрогену є екологічно чистим. 2. Складіть рівняння реакцій сульфур(IV) оксиду з: а) кальцій оксидом; б) кальцій гідроксидом; в) калій карбонатом.
Перехід на альтернативні екологічно чисті джерела енергії (назвіть їх), використання енергозберігальних технологій на виробництві і в побуті - найефективніші заходи запобігання утворенню кислотних опадів.
Цікаво і пізнавально
Виявлено, що пліснявий гриб Stachybotrys chartarum видаляє від 65 % до 76 % сірки із сирої нафти за 30 °С. Новий процес не потребує використання високої температури та великих витрат енергії https://pubs.acs.org/doi/abs/10.1021/ie800494p.
• Поясніть значення цього відкриття в контексті збалансованого розвитку людства.
https://www.youtube.com/watch?v=ynz93H1_2as
https://www.youtube.com/watch?v=1PDjVDIrFec&t=49s
https://www.youtube.com/watch?v=Z5Db5ranTXw
https://www.youtube.com/watch?v=Y6bSKI_o0y8
https://www.youtube.com/watch?v=ccQoSl5buQ4
ПРО ГОЛОВНЕ
• Алгоритм складання назв оксидів за систематичною номенклатурою:
назва хімічного елемента + його валентність1 + оксид.
Приклади: карбон(ІV) оксид, сульфур(VІ) оксид.
• Якщо оксиду неметалічного елемента відповідає кислота - він кислотний, якщо ні - несолетворний.
• Кислотні оксиди добувають спалюванням простих і складних речовин, термічним розкладанням оксигеновмісних кислот та деяких їхніх солей, реакцією обміну між солями й кислотами, солями та кислотними оксидами.
• Продукт реакції кислотного оксиду з водою - кислота, з лугом - сіль і вода, з основним оксидом - сіль.
• Кислотні опади - одна з нагальних екологічних проблем сьогодення.
1 Для хімічних елементів зі змінною валентністю.
Перевірте себе
- 1. Перетворіть розповідні речення з рубрики ПРО ГОЛОВНЕ на запитальні. Чи можете ви відповісти на ці запитання без допомоги підручника?
Застосуйте свої знання й уміння
- 2. Учнівство одинадцятого класу посперечалося. Одні стверджували: щоби вберегти ґрунти від упливу кислотних дощів, достатньо істотно збільшити висоту заводських труб, що викидають кислі промислові гази. Інші заперечували - це не розв’яже проблеми. А як уважаєте ви? Аргументуйте свою думку.
- 3. Учнівство одинадцятого класу не могло дійти згоди щодо кислотних опадів. Одні вважали, що найбільша концентрація катіонів Гідрогену в тумані, другі - у дощі, треті - у хмарах. Долучіться до їхньої дискусії та розташуйте опади за зростанням кислотності. Аргументуйте свою думку.
- 4. Поміркуйте й поясніть, чому озера та річки, розташовані на вапняках, менш зазнають упливу кислотних опадів, ніж ті, що розташовані на гранітах та гнейсах, які переважно складаються з алюмосилікатів.
- 5. Обчисліть: а) об’єм (м3) сульфур(ІV) оксиду(н. у.), який утворився внаслідок згоряння кам’яного вугілля масою 2 т, масова частка Сульфуру в якому - 6,4 %; б) масу (т) вапняку, необхідного для очищення від сульфур(ІV) оксиду продуктів спалювання кам’яного вугілля масою 10 т, масова частка Сульфуру в якому - 3,2 %; в) об’єм (м3) амоніаку, необхідного для каталітичного відновлення суміші об’ємом 1000 м3, яка складається з нітроген(ІІ) оксиду й нітроген(ІV) оксиду. Об’ємна частка нітроген(ІІ) оксиду в суміші становить 40 % (об’єми всіх газів виміряно за однакових умов).
Творча майстерня
- 6. Намалюйте комікс, за допомогою якого можна доступно пояснити актуальність проблеми кислотних дощів.
- 7. Тележурналісту та тележурналістці, які проходять стажування, запропонували підготувати сюжет про проблему кислотних дощів для оптимістично зорієнтованої передачі «Добрі новини». Чи реально виконати таке завдання? Випробуйте себе в цій ролі та напишіть сценарій передачі.
- 8. Складіть перелік ваших простих щоденних дій, які сприятимуть зменшенню утворення кислотних опадів.
Коментарі (0)