Поняття про твердість (жорсткість) води та способи її усунення
- 14-11-2023, 22:55
- 380
11 клас , Хімія 11 клас Лашевська (рівень стандарту)
§ 28. Поняття про твердість (жорсткість) води та способи її усунення
Після опрацювання параграфа ви зможете:
- аналізувати типи твердості води;
- пропонувати безпечні способи усунення твердості води в побуті;
- доводити вплив твердої води на побутові прилади та комунікації.
Твердість води - це сукупність її властивостей, зумовлених деякими катіонами металічних елементів, що містяться в ній. Усі двовалентні катіони тією чи тією мірою впливають на твердість води, оскільки вони взаємодіють з певними аніонами, унаслідок чого утворюються нерозчинні або малорозчинні сполуки, що випадають в осад. Формули найважливіших1 йонів, що зумовлюють твердість води, наведено в таблиці 28.1.
1 Через мізерно малий уміст у воді катіонів Стронцію, Феруму(ІІ) та Феруму(ІІІ), Мангану(ІІ), Барію їхнім упливом на твердість води нехтують.
Таблиця 28.1. Найважливіші йони, які зумовлюють твердість води

Звідки ці йони потрапляють у воду? Їхніми джерелами є природні поклади вапняків (СаСО3), гіпсу (CaSO4 · 2Н2О) і доломіту (СаСО3 · MgCO3). Унаслідок взаємодії розчиненого у воді карбон(ІV) оксиду з мінералами, інших процесів розчинення й хімічного вивітрювання гірських порід природна вода збагачується катіонами та аніонами (рис. 28.1).
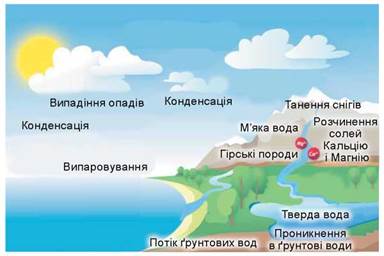
Рис. 28.1. Як м’яка вода стає твердою та навпаки
• Складіть рівняння реакцій між карбонатами Кальцію та Магнію й карбон(ІV) оксидом, розчиненим у воді.
Джерелами йонів, що зумовлюють твердість води, можуть бути мікробіологічні процеси, що відбуваються в ґрунті на площі водозабору, у донних відкладеннях, кислотні опади, а також стічні води підприємств.
Уплив твердої води на побутові прилади, комунікації, організми. Унаслідок нагрівання твердої води в трубах опалювальної системи, кип’ятіння її утворюється осад, який осідає на поверхні нагрівальних елементів, стінках труб, що призводить до зменшення теплопровідності, звужування отворів тощо (рис. 28.2).

Рис. 28.2. Накип у трубі (1) та на поверхні нагрівальних елементів (2)
Використання твердої води призводить до перевитрати електроенергії, бо частину енергії доводиться витрачати на нагрівання шару накипу. У твердій воді зменшується мийна дія мила (натрієвих і калієвих солей стеаратної кислоти) через утворення нерозчинних кальцієвих і магнієвих солей:
2С17Н35СОО- + Са2+ → (С17Н35СОО)2Са↓;
2С17Н35СОО- + Mg2+ → C17H35COO)2Mg↓
Утворені внаслідок цього осади стеаратів Кальцію та Магнію осідають на поверхні шкіри, волосся, заповнюють проміжки між волокнами тканин. Це може призвести до надмірної сухості шкіри, її подразненню. Волосся, вимите милом у твердій воді, тьмяніє та стає ламким. З поверхні тканин, випраних у ній, важче вибавити забруднення та плями. Вапняковий наліт осідає на поверхні облицювальної плитки, керамічних, металевих і пластмасових деталях сантехнічного обладнання (рис. 28.3).
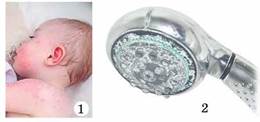
Рис. 28.3. 1. Тверда вода є однією з можливих причин екземи в немовлят. 2. Тверда вода - для сантехніки біда
Цікаво і пізнавально
Інститут колоїдної хімії та хімії води ім. А. В. Думанського Національної академії наук України є єдиною академічною установою, діяльність якої цілком і повністю пов’язана з комплексним дослідженням усіх аспектів хімії й технології води, колоїдної та аналітичної хімії. Одними з найвагоміших досягнень Інституту є розроблення та впровадження технологій та устаткування для одержання якісної питної води
Типи твердості води, їхні причини та способи усунення. Уявлення про них ви зможете дістати, проаналізувавши таблицю 28.2 (зробіть це).
Таблиця 28.2. Твердість води, її типи, причини та способи усунення
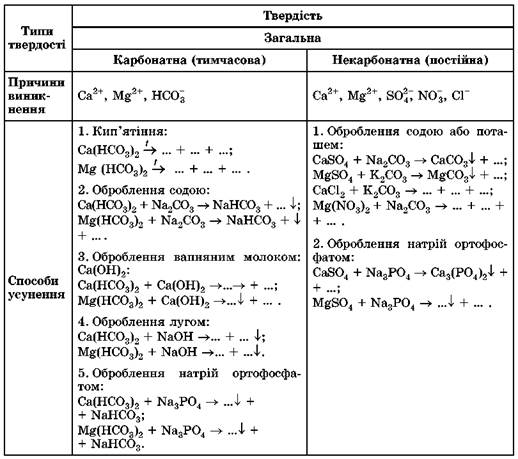
• 1. Перетворіть наведені в таблиці 28.2 схеми реакцій на хімічні рівняння, запишіть відповідні повні й скорочені йонні рівняння. 2. Поясніть: а) чому постійну твердість води не можна усунути кип’ятінням; б) які з наведених у таблиці 28.2 способів зм’якшення води є безпечними для використання в домашніх умовах.
Окрім уже зазначених способів зменшення твердості води, широко використовують й інші. Розгляньмо їх докладніше.
Дистилювання, або термічне опріснення, - чи не найпоширеніший на морських судах спосіб добування прісної води із забортної морської. Також солону воду знесолюють, а отже, і зм’якшують, виморожуванням. Унаслідок охолодження солоної води нижче температури замерзання в ній утворюються кристали льоду - замерзлої прісної води, які відокремлюють від розсолу, промивають і плавлять.
Йонний обмін - одна з найдоступніших та ефективних технологій зм’якшення води, яку пропускають крізь фільтр, що містить йонообмінні смоли. Унаслідок реакцій йонного обміну катіони Кальцію та Магнію з води переходять у смолу, а вода натомість збагачується йонами Натрію. Для регенерування смолу промивають розчином кухонної солі.
Зворотний осмос передбачає використання напівпроникної мембрани, крізь яку під тиском пропускають воду. Мембрана затримує частинки з розмірами 0,001-0,0001 мкм, зокрема гідратовані сульфат-, хлорид- та нітрат-аніони, катіони Натрію, Кальцію, Магнію, молекули барвників тощо, але пропускає молекули води.
Магнітний та електромагнітний методи зм’якшення води. Під час проходження потоку води крізь магнітні та електромагнітні фільтри під дією магнітного поля солі Кальцію та Магнію переходять у нерозчинну форму. Осад, що утворився, з потоком води виводять із системи водопроводу. Таке обладнання застосовують для захисту від накипу котлів, колонок, водонагрівачів, пральних та посудомийних машин у приватних будинках і котеджах.
• Які з наведених вище способів зм’якшення води ґрунтуються на фізичних, а які - на хімічних явищах?
Цікаво і пізнавально
Клітинні оболонки рослини містять пектини - вуглеводні ланцюжки. Пектинову сітку стабілізують йони полівалентних металічних елементів (таких, у яких валентність більша за одиницю). Тобто під час засолювання огірків катіони Кальцію та Магнію роблять пектинову сітку жорсткішою (рис. 28.4), а огірки не розм’якають і стають хрумкими.
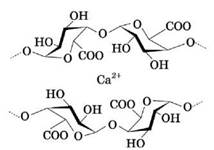
Рис. 28.4
• Поясніть, чому для засолювання огірків досвідчені кулінари й кулінарки радять використовувати: а) для розсолу колодязну чи джерельну воду з підвищеною твердістю або навіть мінеральну воду; б) неочищену кам’яну або морську сіль, а не сіль «Екстра»; в) кальцій хлорид1 як добавку до розсолу; г) лише сиру, а не кип’ячену воду для розсолу.
1 Аптечний препарат.
https://www.youtube.com/watch?v=ebygQes5Wig
https://www.kinetico.co.uk/hard-and-soft-water-explained/hard-and-soft-water-uk
https://www.youtube.com/watch?v=ei-rmud9vBU
ПРО ГОЛОВНЕ
• Твердість води - це сукупність її властивостей, зумовлених катіонами металічних елементів, передусім Са2+ та Mg2+, що є в ній.
• Загальна твердість води складається з карбонатної (тимчасової) та некарбонатної (постійної).
• Карбонатну твердість зумовлено вмістом у воді йонів Са2+, Mg2+, НСО-3, а некарбонатну - Са2+, Mg2+, SO2-4,NO-3, Сl-.
• Карбонатну твердість усувають кип’ятінням і реагентним способом, некарбонатну - реагентним способом.
• Дистилювання, виморожування, йонний обмін, зворотний осмос, магнітний та електромагнітний методи використовують для знесолення й, відповідно, зм’якшення води.
Перевірте себе
- 1. Перетворіть розповідні речення рубрики ПРО ГОЛОВНЕ на питальні. Чи можете ви відповісти на ці запитання без допомоги підручника?
Застосуйте свої знання й уміння
- 2. Розгляньте рисунки 28.5.1 та 28.5.2 й визначте: 1) на якому з його фрагментів - а чи б - зображено посуд, який мили у твердій воді; 2) на якому з його фрагментів - в чи г - зображено колбу з твердою водою, до якої долили мильного розчину й збовтнули.

Рис. 28.5
- 3. Поміркуйте й висловте припущення, чому: а) перегонкою можна усунути як тимчасову, так і постійну твердість води; б) твердість поверхневих вод зазвичай менша від твердості вод підземних; в) твердість поверхневих вод схильна до помітних сезонних коливань і досягає найбільшого значення наприкінці зими й найменшого - у період повені; г) часто систему зворотного осмосу для очищення питної води доповнюють фільтром штучної мінералізації, під час проходження крізь який воду збагачують солями Магнію, Кальцію, Калію, Флуору та інших хімічних елементів до рівня 100 мг/л, а якщо вода призначена для прання та миття посуду, то такий фільтр не встановлюють; д) для чого в посудомийні машини завантажують таблетки, головним складником яких є натрій хлорид, адже він не усуває твердість води та не є мийним засобом.
- 4. За допомогою інтернет-ресурсів знайдіть мапу України, на якій позначено регіони з різною твердістю води. Проаналізуйте й поясніть, чим, на вашу думку, зумовлено відмінності в різних регіонах.
- 5. Проаналізуйте з погляду хімії фрагмент інструкції щодо складу й використання порошку для посудомийних машин: «Лужність розчину, потрібну для процесу миття, забезпечує комбінація натрій карбонату, натрій гідрогенкарбонату, натрій силікату. Натрій цитрат і натрій глюконат зменшують твердість води під час нагрівання її й дають змогу запобігти утворенню осаду на посуді». Чи правильно описав виробник функції кожного зі складників1?
- 6. Запропонуйте способи видалення накипу з огляду на його хімічний склад.
- 7. Доповніть опис досліду: «На предметне скельце нанесли по краплі дистильованої, кип’яченої мінеральної й некип’яченої мінеральної води. Після висихання дистильованої води осад ... . Осад після випаровування кип’яченої мінеральної води дав змогу зробити висновок про її ... твердість, а некип’яченої - про ... ».
1 Візьміть до уваги, що цитрати та глюконати Кальцію й Магнію - малорозчинні сполуки.
Творча майстерня
- 8. Підготуйте презентацію «Тверда та м’яка вода в моєму житті».
Коментарі (0)