Збуджений стан атома. Валентні стани елементів. Можливі ступені окиснення неметалічних елементів другого і третього періодів
- 21-09-2023, 21:29
- 328
11 клас , Хімія 11 клас Лашевська (рівень стандарту)
§ 2. Збуджений стан атома. Валентні стани елементів. Можливі ступені окиснення неметалічних елементів другого і третього періодів
Після опрацювання параграфа ви зможете:
- пояснювати валентність і ступінь окиснення елементів другого та третього періодів в основному й збудженому станах атомів;
- складати електронні формули атомів неметалічних елементів другого та третього періодів в основному й збудженому станах, а також графічні варіанти цих формул;
- порівнювати можливі ступені окиснення розташованих в одній групі неметалічних елементів другого й третього періодів на основі електронної будови їхніх атомів.
Збуджений стан атома. У 9 й 10 класах ви дізналися про основний і збуджений стани атома Карбону та його валентні можливості (мал. 2.1).
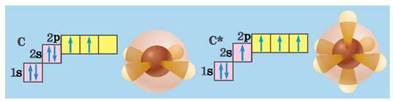
Рис. 2.1. Будова атома Карбону в основному і збудженому станах
Пригадайте: електронні конфігурації атомів з найменшою енергією називають основними. Унаслідок отримання енергії ззовні можливий перехід електронів на вищий підрівень, де є вільні орбіталі. Тобто атом переходить у збуджений стан.
Такий перехід відбувається внаслідок опромінення або нагрівання речовини. Стан, який потребує для підвищення енергії електрона найменших затрат енергії, називають першим збудженим станом. Збуджений стан атома позначають зірочкою - Е*. Наприклад, перший збуджений стан атома Сульфуру зумовлений переходом одного з 3рх-електронів на 3d-підрівень:
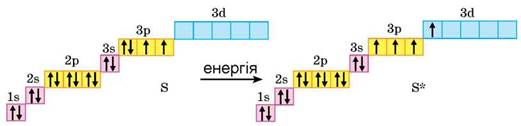
Другий збуджений стан атома Сульфуру зумовлений переходом на 3d-підрівень одного з 3s-електронів:
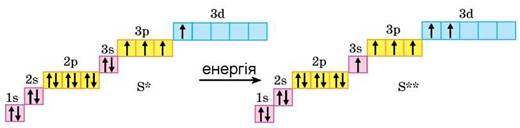
Зверніть увагу: збуджений стан атома - нестійкий. Тому через деякий час електрон, утративши енергію, переходить на енергетичний підрівень з меншою енергією, унаслідок переходу відбувається випромінення фотона - порції (кванта) світла.
Валентні стани елементів та їхні ступені окиснення пов’язані між собою та зумовлені особливостями будови зовнішнього енергетичного рівня атомів. Виконавши завдання, наведені далі, ви зможете дійти щодо цього певних висновків.
1. Сульфур виявляє змінну валентність - II, IV, VI. Проаналізуйте графічні варіанти електронних формул атома Сульфуру в основному й збуджених станах, наведені вище. Скільки неспарених електронів в атомі Сульфуру в кожному із станів? Яким значенням валентності Сульфуру вони, на вашу думку, відповідають? 2. Зобразіть графічний варіант електронної формули атома Оксигену. Чи можливий його перехід у збуджений стан? Чому?
Цікаво і пізнавально
Валентність - багатозначний термін. Наприклад, у мовознавстві - це здатність слова визначати кількість і якість залежних від нього словоформ, зумовлена його семантичними та граматичними властивостями, у психології - позитивна або негативна цінність, значущість об’єкта, події або дії для суб’єкта, їхня мотиваційна (спонукальна) сила.
Порівняймо можливі ступені окиснення розташованих в одній групі неметалічних елементів другого й третього періодів на основі електронної будови їхніх атомів.
1. Зобразіть графічні варіанти електронних формул Флуору та Хлору в основному стані й проаналізуйте їх. Атоми якого із цих двох хімічних елементів можуть перейти в збуджений стан? Чому? 2. Скількох електронів не вистачає атому кожного із цих елементів для набуття стійкої 8-електронної структури - октету? 3. Якого ступеня окиснення набудуть Флуор та Хлор, якщо зовнішні енергетичні рівні їхніх атомів стануть завершеними? 4. Скільки неспарених електронів в атомі Флуору й атомі Хлору в основному стані? 5. Зобразіть графічні варіанти електронних формул атома Хлору в збудженому стані та проаналізуйте їх. 6. Скільки неспарених електронів в атомі Хлору в першому збудженому стані? У другому? У третьому? Скільки електронів може віддати атом Хлору в кожному із цих станів? Якого ступеня окиснення набуде Хлор унаслідок цього? 7. Складіть хімічні формули фторидів Хлору для основного та першого й другого збуджених станів атома Хлору. 8. Визначте ступені окиснення Хлору в речовинах, формули яких СаСl2, Сl2О, NaClO, КСlО3, NaClO2, КСlО4, Сl2.
Знання про будову електронних оболонок атомів хімічних елементів, основний і збуджений стан атомів допоможуть вам зрозуміти, чому багато хімічних елементів виявляють змінну валентність, та глибше усвідомити фізичний зміст явища періодичності, про яке йтиметься в наступному параграфі.
https://www.youtube.com/watch?v=aQZnMIYO8cM
https://www.youtube.com/watch?v=A7nkPaTn3iE&list=UUaFokBdfPtlT5DQaD5a02Hw&index=26
http://toutestquantique.fr/en/quantization/
ПРО ГОЛОВНЕ
• В основному стані енергія електронів в атомі мінімальна.
• Унаслідок отримання енергії ззовні атом може перейти в збуджений стан.
• Збуджений стан атома - нестійкий.
• Валентні стани хімічних елементів та їхні ступені окиснення пов’язані між собою та зумовлені особливостями будови зовнішнього енергетичного рівня атомів.
Перевірте себе
- 1. Перетворіть розповідні речення рубрики ПРО ГОЛОВНЕ на питальні. Чи можете ви відповісти на ці запитання без допомоги підручника?
Застосуйте свої знання й уміння
- 2. Зобразіть графічні варіанти електронних формул атомів елементів другого та третього періодів. Оцініть можливість переходу їхніх атомів у збуджений стан та їхні валентні можливості. Порівняйте кількість збуджених станів у тих з них, що можуть у нього перейти.
- 3. Порівняйте валентні можливості: а) Нітрогену й Фосфору; б) Карбону й Силіцію.
- 4. Спрогнозуйте можливі ступені окиснення неметалічних елементів 2 і 3 періодів, порівняйте їх у межах: а) періодів; б) груп.
Творча майстерня
- 5. Розробіть алгоритм складання графічного варіанта електронної формули атома хімічного елемента.
Коментарі (0)